
Guy-Charles Fanneau de la Horie
Président Directeur Général de Pherecydes
Utiliser les virus prédateurs naturels des bactéries
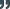
Publié le 22 Janvier 2021
Pour commencer, pouvez-vous nous renseigner brièvement sur Pherecydes Pharma ?
Pherecydes Pharma est une « biotech » créée en 2006. Elle se positionne à l’avant-garde de la phagothérapie, une technique de lutte contre les infections bactériennes les plus résistantes. Nous disposons d’une double implantation en France avec un centre R&D basé à Romainville, et un site de process development et de contrôle qualité situé à Nantes. À ce jour, notre équipe est constituée de 21 collaborateurs.
Plus précisément, et pour des non-spécialistes, qu’est-ce que la phagothérapie ?
Il s’agit d’une solution naturelle pour traiter les infections résistantes, découverte voici près d’un siècle. Pour vaincre les bactéries qui en sont responsables, nous utilisons des bactériophages : ces virus sont en effet les prédateurs naturels des bactéries.-version-a92dcd.png?vh=cf3ec0) Leur principe de fonctionnement est original : une fois administrés sur la zone contaminée, ils repèrent leur cible, se fixent sur elle avant de lui injecter leur ADN. En faisant cela, ils détournent la mécanique de la bactérie pour la retourner contre elle et la tuer, avant de libérer de nouveaux phages.
Leur principe de fonctionnement est original : une fois administrés sur la zone contaminée, ils repèrent leur cible, se fixent sur elle avant de lui injecter leur ADN. En faisant cela, ils détournent la mécanique de la bactérie pour la retourner contre elle et la tuer, avant de libérer de nouveaux phages.
Ce cycle est très rapide, car il dure moins de 45 minutes. Malgré tout, cultiver des phages est tout sauf simple, à la fois pour réussir à les produire et pour leur garantir une qualité irréprochable.
L’utilisation des phages présente-elle une forme de risques ou d’effets secondaires pour le patient ?
Absolument aucun. Ces bio-organismes sont très spécifiques et n’ont aucune activité sur les cellules humaines et animales. Autre aspect très intéressant de la phagothérapie : l’autoréplication naturelle des phages au contact des bactéries. Pas besoin d’administration répétée, le traitement fonctionne dès la première application. L’expérience acquise auprès de 22 patients déjà traités, dans le cadre de traitements compassionnels délivrés au sein de centres hospitaliers reconnus, démontre que la technique est simple, efficace et bien tolérée.
Quelle est la spécificité de l’approche retenue par Pherecydes Pharma ?
Tout d’abord, nous avons fait le choix de nous focaliser sur la récolte d’organismes vivants évoluant dans un environnement naturel. Par exemple les réseaux d’égouts à proximité des hôpitaux, où l’on retrouve aussi sans surprise les bactéries les plus dangereuses… Notre approche innovante, c’est celle de la phagothérapie de précision. Nous avons ainsi choisi trois familles de phages permettant de traiter 68% des infections nosocomiales en s’attaquant aux trois bactéries les plus dangereuses pour l’homme selon l’OMS : Staphylococcus aureus, Pseudomonas aeruginosa et Escherichia coli. En fonction de la cible, nous sélectionnons le phage adéquat parmi nos différents champions. Les capacités de ces derniers ont été évaluées rigoureusement, notamment sur la base de leur efficacité sur un grand nombre de souches et de leurs bons rendements de production. Nous travaillons ensuite à rendre ces champions les plus purs et efficaces possible. Enfin, nous appliquons un seul type de phage à la fois, celui dont l’action spécifique permet de détruire la souche ciblée.
Quelle méthode de mise en application concrète suivez-vous ?
Concrètement, dans le cadre de traitements compassionnels*, nous avons répondu sous le contrôle de l’ANMS aux hôpitaux qui en ont fait la demande. La méthode est toujours la même : à partir d’un échantillon de la bactérie cible prélevée sur le patient, nous réalisons en deux jours une analyse nommée Phagogramme. Elle nous permet ensuite d’assembler les phages adaptés dans une solution physiologique qui est envoyée à l’hôpital pour administration au patient. Dans les 22 cas concernés, la solution apportée s’est avérée à chaque fois efficace.
Où en êtes-vous dans le processus menant à l’autorisation de mise sur le marché ?
La spécificité du savoir-faire de Pherecydes Pharma se concrétise pour le moment dans les quatre brevets déposés par l’entreprise, dont certains délivrés en Europe, aux États-Unis, au Japon, à Hong-Kong et en Australie. Notre première famille de phages, qui vise la Staphylococcus aureus, entrera en étude de phase 1/2 mi-2021. La seconde, qui adresse des indications à forte mortalité causées par la Pseudomonas aeruginosa, s’appuie sur une souche bactérienne génétiquement modifiée et fait l’objet de brevets en cours de développement. Enfin, la troisième vise la Escherichia coli, principale source d’infections nosocomiales, et deux études sont envisagées à son sujet. Globalement les projections nous font espérer, en fonctions des résultats intermédiaires, une autorisation de mise sur le marché à l’horizon 2025.
Dans quel domaine d’action plus large s’inscrit la phagothérapie ?
Nous vivons depuis la fin des années 1980 quelque chose qu’avait prédit Alexander Fleming, l’inventeur de la pénicilline : l’antibiorésistance est devenue un enjeu de santé publique critique et planétaire. Tout simplement, depuis cette époque, aucune nouvelle classe d’antibiotiques n’a été commercialisée. Et les bactéries se sont adaptées, causant en 2014 près de 700 000 morts dans le monde. Ce chiffre s’accroît dramatiquement, à tel point qu’il devrait atteindre 10 millions de morts en 2050. C’est dire l’importance stratégique de trouver une alternative dans la lutte contre les bactéries, une problématique médicale déjà synonyme de lourdes conséquences financières. Par exemple, pour 2022, on anticipe aux États-Unis un chiffrage des pathologies liées à l’antibiorésistance de l’ordre de 36 milliards de dollars.
En termes de marché, dans quel environnement se situe Pherecydes Pharma ?
Pour toutes les raisons évoquées à l’instant, sur un marché porteur marqué par une prise de conscience accrue de l’urgence de la situation. Celle-ci apparaît dans l’intérêt médiatique actuel pour la phagothérapie, et en miroir dans les publications scientifiques sur le sujet, en forte hausse depuis le début des années 2000. Bien entendu, nous ne sommes pas la seule entreprise spécialisée dans ce domaine. Chacune se singularise par des cibles et des approches différentes, production naturelle ou synthétique, à visée microbiotique ou antibiotique, etc. Sur ce marché, Pherecydes Pharma se positionne comme leader du développement de phages naturels dédiés à l’antibiorésistance.
À quels objectifs répond votre entrée en bourse sur Euronext Growth, lancée le 20 janvier ?
Nous visons une augmentation de capital de 7 millions d’euros, à raison d’un prix unitaire ferme de 6 €. De quoi poursuivre sereinement le travail d’élaboration de notre phagothérapie de précision et la poursuite des objectifs de développements cliniques. Nous abordons en effet une période d’essais essentielle au développement de nos produits dans un contexte marqué par une vraie urgence sanitaire. C’est donc le moment pour Pherecydes Pharma d’accroître ses capacités financières afin notamment d’assumer les nouveaux coûts afférents à cette étape. Ils seront portés également par la commercialisation de certains produits concernés par des autorisations temporaires d’utilisation à partir du deuxième semestre 2021, et par des fonds publics mobilisés notamment dans la réalisation de deux études. Tout ceci en cohérence avec la stratégie mise en place depuis la création de l’entreprise : limiter le risque autant que possible.
Aymeric Jeanson
* Pour un malade, rien n'est pire sur un plan psychologique et humain que de sentir ses capacités s'affaiblir ou d'avoir à affronter la mort alors que des traitements expérimentaux existent quelque part, dans l'attente d'une évaluation finale. De nos jours, les malades sont parfaitement informés des nouveaux médicaments mis au point. Dans certains pays, le législateur a remédié à cette situation en rendant les médicaments accessibles dans le cadre d'un usage compassionnel, avant l'autorisation de mise sur le marché. Cette démarche permet de traiter des malades qui n'ont aucun autre recours et qui n'ont pas non plus le temps d'attendre la fin des essais cliniques et du processus d'autorisation.
Pherecydes Pharma est une « biotech » créée en 2006. Elle se positionne à l’avant-garde de la phagothérapie, une technique de lutte contre les infections bactériennes les plus résistantes. Nous disposons d’une double implantation en France avec un centre R&D basé à Romainville, et un site de process development et de contrôle qualité situé à Nantes. À ce jour, notre équipe est constituée de 21 collaborateurs.
Plus précisément, et pour des non-spécialistes, qu’est-ce que la phagothérapie ?
Il s’agit d’une solution naturelle pour traiter les infections résistantes, découverte voici près d’un siècle. Pour vaincre les bactéries qui en sont responsables, nous utilisons des bactériophages : ces virus sont en effet les prédateurs naturels des bactéries.
-version-a92dcd.png?vh=cf3ec0)

Ce cycle est très rapide, car il dure moins de 45 minutes. Malgré tout, cultiver des phages est tout sauf simple, à la fois pour réussir à les produire et pour leur garantir une qualité irréprochable.
L’utilisation des phages présente-elle une forme de risques ou d’effets secondaires pour le patient ?
Absolument aucun. Ces bio-organismes sont très spécifiques et n’ont aucune activité sur les cellules humaines et animales. Autre aspect très intéressant de la phagothérapie : l’autoréplication naturelle des phages au contact des bactéries. Pas besoin d’administration répétée, le traitement fonctionne dès la première application. L’expérience acquise auprès de 22 patients déjà traités, dans le cadre de traitements compassionnels délivrés au sein de centres hospitaliers reconnus, démontre que la technique est simple, efficace et bien tolérée.
Quelle est la spécificité de l’approche retenue par Pherecydes Pharma ?
Tout d’abord, nous avons fait le choix de nous focaliser sur la récolte d’organismes vivants évoluant dans un environnement naturel. Par exemple les réseaux d’égouts à proximité des hôpitaux, où l’on retrouve aussi sans surprise les bactéries les plus dangereuses… Notre approche innovante, c’est celle de la phagothérapie de précision. Nous avons ainsi choisi trois familles de phages permettant de traiter 68% des infections nosocomiales en s’attaquant aux trois bactéries les plus dangereuses pour l’homme selon l’OMS : Staphylococcus aureus, Pseudomonas aeruginosa et Escherichia coli. En fonction de la cible, nous sélectionnons le phage adéquat parmi nos différents champions. Les capacités de ces derniers ont été évaluées rigoureusement, notamment sur la base de leur efficacité sur un grand nombre de souches et de leurs bons rendements de production. Nous travaillons ensuite à rendre ces champions les plus purs et efficaces possible. Enfin, nous appliquons un seul type de phage à la fois, celui dont l’action spécifique permet de détruire la souche ciblée.
Quelle méthode de mise en application concrète suivez-vous ?
Concrètement, dans le cadre de traitements compassionnels*, nous avons répondu sous le contrôle de l’ANMS aux hôpitaux qui en ont fait la demande. La méthode est toujours la même : à partir d’un échantillon de la bactérie cible prélevée sur le patient, nous réalisons en deux jours une analyse nommée Phagogramme. Elle nous permet ensuite d’assembler les phages adaptés dans une solution physiologique qui est envoyée à l’hôpital pour administration au patient. Dans les 22 cas concernés, la solution apportée s’est avérée à chaque fois efficace.
Où en êtes-vous dans le processus menant à l’autorisation de mise sur le marché ?
La spécificité du savoir-faire de Pherecydes Pharma se concrétise pour le moment dans les quatre brevets déposés par l’entreprise, dont certains délivrés en Europe, aux États-Unis, au Japon, à Hong-Kong et en Australie. Notre première famille de phages, qui vise la Staphylococcus aureus, entrera en étude de phase 1/2 mi-2021. La seconde, qui adresse des indications à forte mortalité causées par la Pseudomonas aeruginosa, s’appuie sur une souche bactérienne génétiquement modifiée et fait l’objet de brevets en cours de développement. Enfin, la troisième vise la Escherichia coli, principale source d’infections nosocomiales, et deux études sont envisagées à son sujet. Globalement les projections nous font espérer, en fonctions des résultats intermédiaires, une autorisation de mise sur le marché à l’horizon 2025.
Dans quel domaine d’action plus large s’inscrit la phagothérapie ?
Nous vivons depuis la fin des années 1980 quelque chose qu’avait prédit Alexander Fleming, l’inventeur de la pénicilline : l’antibiorésistance est devenue un enjeu de santé publique critique et planétaire. Tout simplement, depuis cette époque, aucune nouvelle classe d’antibiotiques n’a été commercialisée. Et les bactéries se sont adaptées, causant en 2014 près de 700 000 morts dans le monde. Ce chiffre s’accroît dramatiquement, à tel point qu’il devrait atteindre 10 millions de morts en 2050. C’est dire l’importance stratégique de trouver une alternative dans la lutte contre les bactéries, une problématique médicale déjà synonyme de lourdes conséquences financières. Par exemple, pour 2022, on anticipe aux États-Unis un chiffrage des pathologies liées à l’antibiorésistance de l’ordre de 36 milliards de dollars.
En termes de marché, dans quel environnement se situe Pherecydes Pharma ?
Pour toutes les raisons évoquées à l’instant, sur un marché porteur marqué par une prise de conscience accrue de l’urgence de la situation. Celle-ci apparaît dans l’intérêt médiatique actuel pour la phagothérapie, et en miroir dans les publications scientifiques sur le sujet, en forte hausse depuis le début des années 2000. Bien entendu, nous ne sommes pas la seule entreprise spécialisée dans ce domaine. Chacune se singularise par des cibles et des approches différentes, production naturelle ou synthétique, à visée microbiotique ou antibiotique, etc. Sur ce marché, Pherecydes Pharma se positionne comme leader du développement de phages naturels dédiés à l’antibiorésistance.
À quels objectifs répond votre entrée en bourse sur Euronext Growth, lancée le 20 janvier ?
Nous visons une augmentation de capital de 7 millions d’euros, à raison d’un prix unitaire ferme de 6 €. De quoi poursuivre sereinement le travail d’élaboration de notre phagothérapie de précision et la poursuite des objectifs de développements cliniques. Nous abordons en effet une période d’essais essentielle au développement de nos produits dans un contexte marqué par une vraie urgence sanitaire. C’est donc le moment pour Pherecydes Pharma d’accroître ses capacités financières afin notamment d’assumer les nouveaux coûts afférents à cette étape. Ils seront portés également par la commercialisation de certains produits concernés par des autorisations temporaires d’utilisation à partir du deuxième semestre 2021, et par des fonds publics mobilisés notamment dans la réalisation de deux études. Tout ceci en cohérence avec la stratégie mise en place depuis la création de l’entreprise : limiter le risque autant que possible.
Aymeric Jeanson
* Pour un malade, rien n'est pire sur un plan psychologique et humain que de sentir ses capacités s'affaiblir ou d'avoir à affronter la mort alors que des traitements expérimentaux existent quelque part, dans l'attente d'une évaluation finale. De nos jours, les malades sont parfaitement informés des nouveaux médicaments mis au point. Dans certains pays, le législateur a remédié à cette situation en rendant les médicaments accessibles dans le cadre d'un usage compassionnel, avant l'autorisation de mise sur le marché. Cette démarche permet de traiter des malades qui n'ont aucun autre recours et qui n'ont pas non plus le temps d'attendre la fin des essais cliniques et du processus d'autorisation.
_



 PLUS DE 20 000 PRODUITS À 0 DE FRAIS DE COURTAGE
PLUS DE 20 000 PRODUITS À 0 DE FRAIS DE COURTAGE